创新药市场正经历一场痛苦的回调,寒冬一词席卷街头巷陌,核药却逆势翻红,成为寒冬中的一抹亮色。
2023年12月底,跨国生物医药巨头百时美施贵宝(BMS)宣布以41亿美元溢价收购核药新锐RayzeBio,超过RayzeBio IPO定价的三倍,一举成为2023年核药赛道*并购案。
如果说BMS超百亿元收购,让人看到Biotech踩中核药赛道,一飞冲天的致富故事。那么礼来以14亿美元、溢价68%的交易,收购了Point Biopharma;罗氏旗下基因泰克与PeptiDream达成一项超10亿美金合作协议,旨在发现和开发新型大环肽-放射性同位素(肽-RI)等事件,无不昭示着MNC重金押注核药赛道的决心。
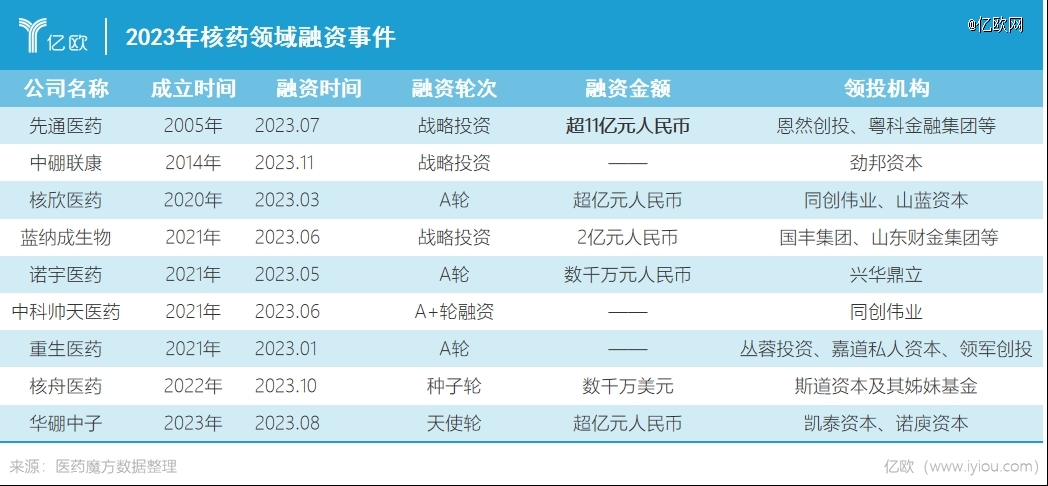
二级市场的欣欣向荣也点燃了一级市场的投资热情,核药企业备受资本追捧,5年时间,美国核药风险投资交易增长了550%。回归国内视角来看,2023年7月,先通医药获得超11亿元融资,成为中国国内医疗健康领域2023年*的一笔融资,傲视群雄。根据医药魔方数据库,2023年国内有11家核药企业获得融资,已披露总金额创下新高,达到了17.5亿元。
种种迹象,无不表示在中国,这个沉寂多年的核药市场早已呼啸而起,成为下一个流淌着奶与蜜之地。核药究竟缘何复兴?有哪些仍待解决的问题?
01、RDC成治疗性核药中“最亮的崽”
核药,依据使用范围可分为体内核药与体外核药。体外核药指利用同位素放射性特征进行标记的免疫诊断试剂,体内核药按临床用途又可分为诊断类核药与治疗类核药。
其中,放射性核素偶联药物(RDC)则是冉冉升起的一颗新星,为业界公认*潜力、效果*的研发方向,诺华、礼来、拜耳等MNC豪掷千金在此布局。
与吸金*ADC结构类似,RDC主要由介导靶向定位作用的抗体或小分子、连接臂、螯合物和放射/成像因子(放射性同位素)构成。 它药物载荷为放射性核素,构成了和其他偶联药物之间*的差异。
简而言之,RDC相当于为核素装上导航系统,在人体中精准投送至特定细胞。放射能量小、半衰期短的核素可以用于显像,精准找到病灶。扫描后,将RDC上装载的诊断显像用同位素换成具有治疗作用的同位素,即可实现影像诊断和治疗的“一条龙服务”。
可视化诊疗,技术的突破使得RDC近乎成为核药代名词,弄潮者诺华以Pluvicto一己之力拉升商业化想象空间。
2022年3月,Pluvicto获得FDA批准,用于PSMA阳性转移性去势抵抗性前列腺癌三线治疗。上市仅一年,热销程度就远超华尔街想象,因为产能无法满足患者需求,诺华一度停止了为Pluvicto接收新患者。
即便如此,Pluvicto还是创造了2023年前三季度销售7.07亿美元的战绩。不出意外,*商业化完整年度,它便能如愿迈进“重磅炸弹”行列。在生产基地扩建的同时,诺华还将该款产品的销售预期上调至30亿美元。
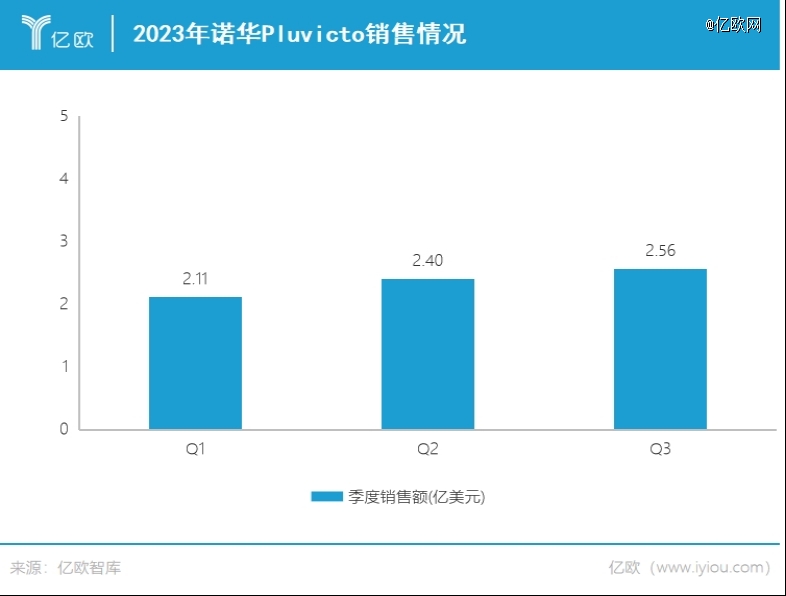
Pluvicto的风光无限,不仅直接,也让众多药企、资本心生向往。RDC赛道青云直上,成为聚光灯下的制药宠儿。
一级市场首先热了起来。分拆自RayzeBio的艾博兹医药,于2021年底完成7500万美元融资;辐联科技更是引得红杉中国、楹联健康基金、佳辰资本入场,2024年1月5日又宣布获得6330万美元;而开发出中国核医学领域*自主研发I类创新药的瑞迪奥也获得了百洋医药集团的战略投资……
有机构统计,中国放射性显像诊断和治疗用药物市场规模已经从2017年的22亿元增至2021年的30亿元,预计2030年市场规模将达到260亿元人民币。
02、恒瑞、远大抢占,核药竞争日趋升温
疗效及“印钞机”般的业绩,是吸引众多药企及资本重金押注的关键。
核药双寡头——中国同辐和东诚药业凭借先天优势,核药房布局国内*,以自研+并购双管齐下构建诊疗核药丰富管线。
恒瑞医药作为创新药一哥,亦对核药领域发起冲击。2023年开年,恒瑞的镥[177Lu]氧奥曲肽注射液获得临床试验批准,其为诺华Lutathera的me—too药。这款产品填补了恒瑞肿瘤管线核素精准治疗的空白。此后,HRS-9815注射液、HRS-4357注射液相继获批临床,不难看出一哥对核药赛道的志在必行。
2023年8月14日,远大医药宣布,用于诊断前列腺癌的全球创新放射性核素偶联药物TLX591-CDx国内III期临床试验已完成首例患者入组给药。核药抗肿瘤诊疗板块是远大医药重点布局的战略领域之一,围绕肿瘤诊疗一体化,远大医药已储备了13款创新产品,涵盖6种放射性核素。
9月,科伦博泰以3580万元人民币的首付款和里程碑付款引进西南医科大学附属医院骨靶向放射性偶联药物TBM-001,拉开了进军核药的帷幕。
相较于治疗性核药,诊断性核药发展较早,步伐迈得更为大步。2023年9月15日,Aβ-PET显像剂欧韦宁®氟[18F]贝他苯注射液获NMPA批准,可实现早期、精准、无创的阿尔茨海默病(AD)诊断,成为国内*获批用于阿尔兹海默诊断的Aβ-PET显像剂。
截至2023年10月,已经有42款放射性药物获NMPA批准上市,其中24款放射性药物仅用于诊断、15款放射性药物仅用于治疗、3款放射性药物既用于诊断也用于治疗。
同期,中国有32款放射性药物处于临床试验及申请上市阶段,其中24款为诊断用放射性药物、8款为治疗用放射性药物。
在研的24款放射性药物中,其中4款药物为RDC,分别为恒瑞医药的镓[68Ga]依度曲肽、Telix的TLX591 CDx、远大医药的锆[89Zr]吉伦妥昔单抗,以及瑞迪奥用于SPECT/CT肿瘤显像剂99mTc-3PRGD2 。
热浪,已经扑面而来。
03、壁垒高耸,不是谁都能卷入的战斗
“现在下手太晚了,容量有限。”一投资人在谈及核药赛道时向亿欧大健康如此说道。
核素的放射性和半衰期,注定了核药的开发和市场布局迥异于一般药物。风险性,决定了其在研发、生产和经营的过程中,受到多方面特殊监管,有着令人望而生畏的进入壁垒。
从核药产业链上游来说,医用放射性核素大多来自核反应堆制备,所占比例超过八成。而国内反应堆生产同位素较少,国内反应堆、加速器等来源的创新核素分离纯化技术以及GMP生产供应等仍旧需要新的技术突破,放射性核素原料依赖于进口。
“排实验时要完全跟着核素供应走,摆脱不了供应周期,供应非常缺乏弹性。”一业内人士曾在直播中如此指出,随着核素国产化、地产化,问题可能会得到逐步缓解。
中游研发阶段,符合多个部门要求的实验场所有限,配套仪器设备有效,还未有完善的生态链。
历经艰难险阻,到了下游应用端,医疗机构开展核素治疗工作需要按照国家相关部门和相关法律法规的要求取得《放射性工作诊疗许可证》《放射性药物使用许可证》和《辐射安全许可证》,相关工作人员要取得专业资质、执业许可并通过从事核医学工作的相关培训才能上岗。
目前,全国能够开展核医学诊疗工作的科室仅为1148个,拥有核素治疗病房的医院约340个,开展核素治疗工作的医院736个,远远不能满足患者的医疗需求。
核药沉寂多年,再次翻红的发展轨迹中,藏着若干桎梏的缩影。而现在,翻红的核药已经有了同质化趋势,具备明显临床优势的靶点相对较集中。
药渡数据指出,当前核药行业靶点同质化,内卷严重,主要集中在PSMA(前列腺特异性膜抗原)和SSTR(生长抑素受体)两个靶点。仅国内30余家核药企业中,PSMA就有19个在研项目(7个IND), Dotatate十余个(5个IND)。而前列腺癌在国内为小癌种,神经内分泌肿瘤为罕见病。
“可能我们现在看到的是,有的靶点同质化严重,但也许每个公司都有自己的差异化考虑,看上去很卷,实际上并不卷。”艾博兹医药高级副总裁、CMC负责人温剑锋博士在公开直播中表示,核药其实是一种组合创新,它是放疗+精准递送(抗体、多肽、小分子、纳米微球)技术的组合。所以核药的开发涉及了很多环节,每个环节都是有可创新的地方,不仅仅是靶点。
研发之难、印钞机般的造富速度共同构成了核药领域跌宕起伏的传奇。在政策春风吹拂下,各方合力打通生产供应、生产流通、临床应用、医院准入等环节关卡,下一个重磅炸弹或许就在中国药企中产生。
【本文由投资界合作伙伴亿欧网授权发布,本平台仅提供信息存储服务。】如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。