6月25日,沃森生物发布公告:公司与艾博生物签署《终止协议》,终止新冠mRNA疫苗和带状疱疹mRNA疫苗的技术开发合作;合作终止后,各方将对前期研发、临床等相关费用进行结算。
这也不是沃森生物今年*次“止损”管线了。
今年4月和6月早些时间,沃森生物分别终止了子公司微达生物的重组新型冠状病毒疫苗(黑猩猩腺病毒载体)临床、子公司泽润生物重组新型冠状病毒疫苗(CHO细胞)及变异株新冠疫苗(CHO细胞)的临床。
如此一来,沃森生物将体内的新冠疫苗管线几近做了“大扫除”,五大新冠疫苗管线并行的时代已成为历史。
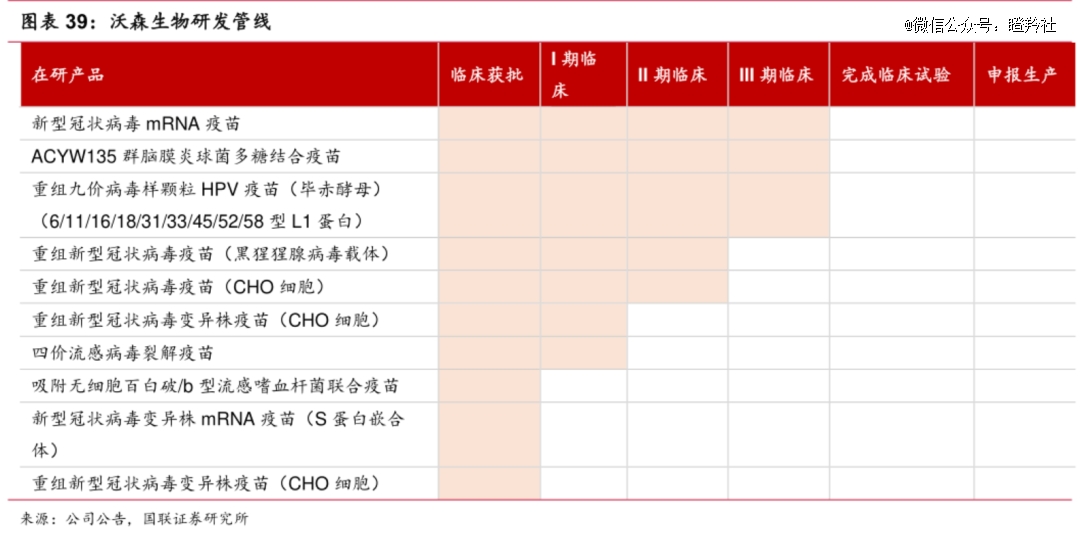
话说回来,早有明眼人预见:沃森生物和艾博生物早已貌合神离。
早在2020年沃森生物就与艾博生物开展合作,而在2022年初沃森生物同时宣布与另一家mrna疫苗研发厂商蓝鹊生物开发新一代mrna新冠疫苗时,市场就有对双方合作“闹掰”的传闻。
沃森生物/艾博生物合作的艾可欣(ARCoVax)2020年6月获得国内临床批件,但后来迟迟未能获得国内批准,仅仅2022年9月在印尼获得紧急使用授权。
无论是原有合作管线不及预期也好,还是双方存在内部矛盾也好,双方合作内容已成空架子,合作终止只差一纸官宣。
从最新的沃森生物投资者问答交流情况看,沃森生物与蓝鹊生物合作仍在持续,合作产品包括:新冠变异株mRNA疫苗、呼吸道合胞病毒mRNA疫苗、流感病毒mRNA疫苗。
01 沃森生物“寻枪”失败
沃森生物可谓是屋漏偏逢连夜雨。
当时为了坐上新冠这趟顺风车,公司耗费了巨资。自2020年之后,2021-2023年沃森生物的研发费用大幅增加,研发费用分别为6.22亿、9.33亿和7.76亿。以2021年为例,沃森生物在mRNA新冠疫苗研发支出高达3.26亿元,超过了当年的研发支出的一半。同时,为了配套mRNA疫苗的商业化生产,沃森生物还在玉溪高新区疫苗产业园建立了年产能2亿剂生产基地,耗资5.2亿元。
在新冠疫苗上,*修成正果的是与蓝鹊生物合作的新冠变异株mRNA疫苗,在2023年底获得国内紧急使用授权,可惜市场已经消失。
沃森生物的基本盘也在遭受国内激烈竞争环境下带来的考验。
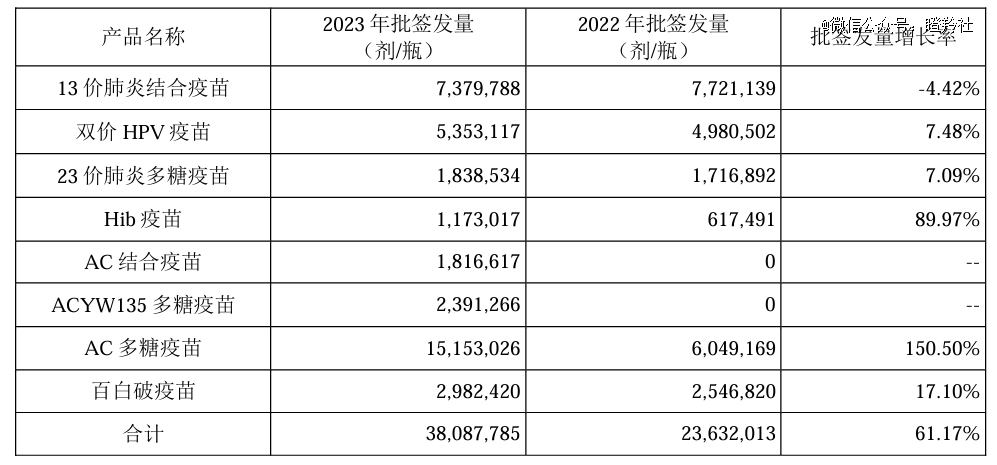
自2020年以来,沃森生物的13价肺炎疫苗是公司最主要的核心收入来源,随着2022年公司二价HPV疫苗投入商业化吃到了国产第二名的红利,推动沃森生物2022年达到了一个收入的小高潮,规模达到50.86亿元,2020-2022年收入CARG高达31.55%。
可惜好景不长,以2023年的批签发量审视,13价肺炎疫苗批签发量同比下降4.42%,公司解释是受国内新生儿数量下降和市场竞争加剧等因素影响;更严峻的是,尽管二价HPV疫苗批签发量录得同比增长,但受到九价HPV疫苗扩龄和进口数量大幅增加、产品大幅降价等因素影响,批签发量的增加幅度并不能覆盖二价HPV疫苗的营收规模损失。
其实也能够理解沃森生物对于整合和扩张自家管线的急迫性,公司急需全新的增长点来支撑公司业绩,经此一整合清理,公司进入临床三期且有大品种潜力的管线仅有9价HPV疫苗,待到真正上市后或许又将重演二价HPV内卷价格战的发展历程。
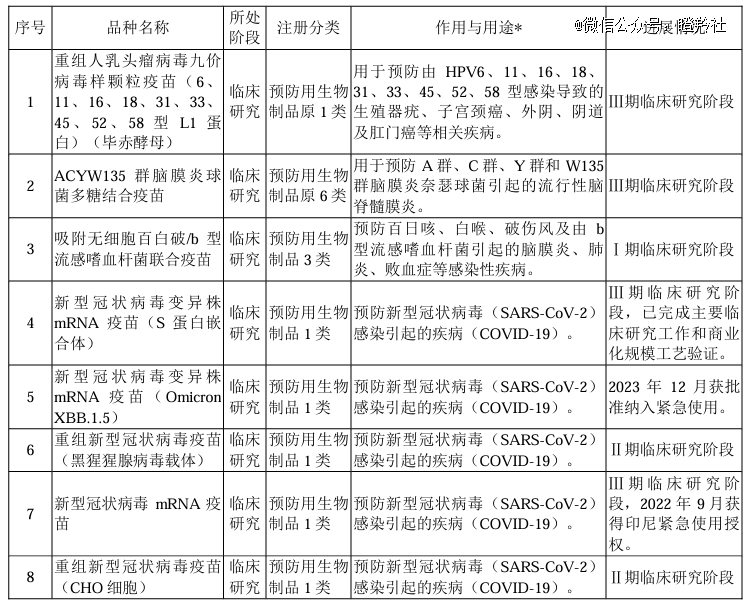
所以,公司急切且不惜重金“寻枪”布局mRNA技术,可以算是对这一未来主流技术领域的看好,布局品种包括呼吸道合胞病毒疫苗、流感疫苗、带状疱疹疫苗等。
02 艾博生物“伤仲永”
事件的另一个主角艾博生物的境况,也一言难尽。
艾博生物的累计融资金额高达11亿美元,比斯微生物规模更大,但其并没有走上“挥霍、濒临倒闭”的道路。而经历了斯微这一事件后,相信艾博一级的股东们首要任务可能是加强对公司财务的管理,以防资金以各种理由“悄悄逃走”。
自艾博生物研发新冠疫苗艾可欣(ARCoVax)无果以来,市场上几乎很难听到来自公司拓展其他新管线的消息。
艾博生物mRNA技术应用有两条线,一是传染病防治领域,这个领域除了新冠疫苗外到目前再无新的管线进入临床;二是肿瘤领域,2023-2024年公司*在药品审评中心备案受理临床的品种只有一款ABO-2011,其余显示进入临床的均为研究者发起的ITT试验。

艾博生物进入临床阶段的ABO2011是一款编码细胞因子IL-12mRNA的脂质纳米球注射液,通过表达IL-12蛋白,激活免疫细胞以发挥抗肿瘤活性,首次临床申报适应症为系统化标准治疗后进展或转移的晚期实体瘤。
对于艾博生物来说,专注于肿瘤疫苗领域未必是一件坏事,既能*程度留存现金,又能规避摊子铺的太大导致的管线失败价值破灭风险。只不过这样一来,公司相关产品要进入商业化阶段,可能至少要等到5年后。莫德纳的mRNA-4157有望成为全球*获批的mrna肿瘤疫苗,其进入临床到上市,预估要花费5-6年时间。
岁月蹉跎下,艾博生物很大可能泯然众人矣。
03 眼看海外mRNA崛起
海外公司的mRNA技术正在积极的攻克除新冠以外的适应症,进展最快的便是呼吸道传染病领域。
以mRNA技术巨头莫德纳为例,其RSV疫苗mRNA-1345在近期获得FDA批准,成为第三款FDA批准的RSV疫苗和*款mRNA RSV疫苗,并且刚刚公布有效率为50%。
另外,莫德纳的季节性流感疫苗mRNA-1010已经在三项三期临床中达到所有免疫原性终点,预计今年年内向FDA递交上市申请。
利用成熟的技术基础,莫德纳还在快速推进“多联苗”项目,计划2025年推出“流感+新冠”组合疫苗,2026年可能推出“新冠+流感+RSV”三联疫苗。
而肿瘤疫苗也是时下一个热门mRNA技术研发路径的选择。
默沙东/Moderna的个性化肿瘤疫苗mRNA-4157(V940)最新公布的一项联合K药用于完全切除后的高危III/IV期黑色素瘤的一项IIb期研究三年随访数据显示:相比K药对照组,联合治疗组患者复发或死亡风险降低了49%,远处转移或死亡的风险降低了62%。另外,联合治疗组的2.5年无复发生存率更高,为74.8%,而单独使用K药为55.6%。
BioNTech/基因泰克的个性化肿瘤疫苗BNT122更“强悍”,瞄准的是“癌王”胰腺癌,在《Nature》报道的BNT122一期数据显示:28例已接受手术治疗的患者中,19例术后给予阿替利珠单抗,其中16例随后输注BNT122疫苗,15例患者之后还给予mFOLFIRINOX(改良版四药化疗方案),8例无应答患者的中位无复发生存时间(RFS)长达13.4个月,这意味着加入BNT122治疗术后胰腺癌患者有潜力降低复发风险、延长患者的生存时间。
海外各个mRNA巨头正在攻城略地,反观国内,产品布局和技术平台令人惊艳稀缺Biotech,而布局mRNA疫苗进度方面反而让石药这样的Pharam走在了领域的前沿,这一背景值得深思。
结语:国内疫苗厂商们“躺赚传统”使得行业积弊已久,同时这也一定程度上占用了后续新兴Biotech的资源,随着这一波疫苗品种洗牌期的来临,希望能让国内的疫苗创新上一个台阶。
【本文由投资界合作伙伴微信公众号:瞪羚社授权发布,本平台仅提供信息存储服务。】如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。





