MNC巨头们在围攻一个“光明顶”。
这个“光明顶”恰恰是血友病领域,作为近20年来FDA批准的*用于治疗A型血友病的创新药,罗氏艾美赛珠单抗Hemlibra自2018年上市以来保持了强劲的增长表现,2023年销售峰值继续攀爬达到45.95亿美元。
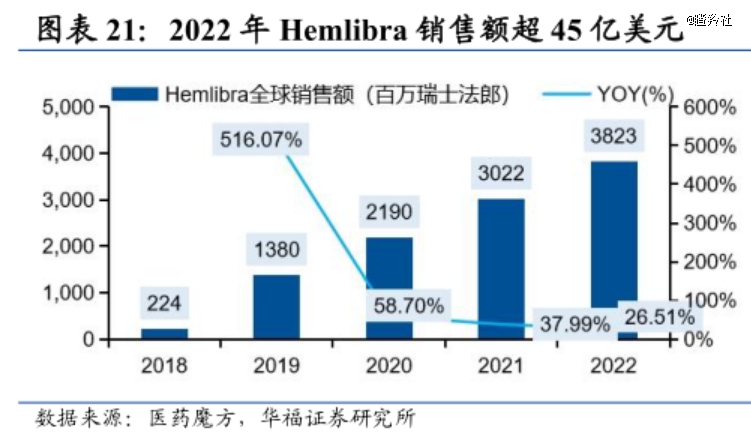
Hemlibra的稳健表现也仅仅是血友病治疗药物庞大市场的冰山一角,Hemlibra作为人凝血因子VIII的替代疗法,凝血因子VIII产品拥有更大的市场规模,数据显示2022年全球人凝血因子VIII市场规模约665亿元(折合约93亿美元)。
罗氏Hemlibra通过一周一次皮下注射的便捷性,迅速在血友病A治疗领域站稳脚跟,这也引发了其他MNC巨头的觊觎。
8月13日,辉瑞治疗血友病的TFPI抗体国内递交上市申请(去年12月已在欧美递交上市申请),与公司的B型血友病基因疗法Beqvez、已经在关键临床取得积极结果的A型血友病基因疗法PF-07055480构成了强劲的产品管线组合,未来将对市场发起猛烈冲击。
觊觎的同样还有诺和诺德,早在2019年其长效重组凝血因子Ⅷ注射用培妥罗凝血素α已经在美国获批上市(近日又在国内获批,每4天一次注射);诺和诺德更大的杀招在后头,其一款针对FIXa和FX的双抗mim8被认为最有望冲击Hemlibra地位的重磅炸弹,预计将在2024年内申报上市;另外,公司TFPI单抗已在加拿大和日本获批上市,不过该产品因需补充信息暂被FDA拒之门外。
血友病这一市场,到底有何魅力?我们拨开迷雾。
1、血友病市场
血友病是X染色体连锁的隐性遗传性疾病,主要可分为血友病A和血友病B,血友病A是因为凝血因子VIII缺乏而引起的出血性疾病,B型血友病则是因为FⅨ缺乏。以血友病A为例,其占到血友病患者的八成以上,如若反复出血不及时治疗,可导致关节畸形或假肿瘤形成,严重者可危及生命。
目前,替代治疗是血友病A的主要治疗方法之一,通过定期输注外源性的凝血因子补充来减少出血时的不良预后,其中使用最多的就是VIII因子药物。
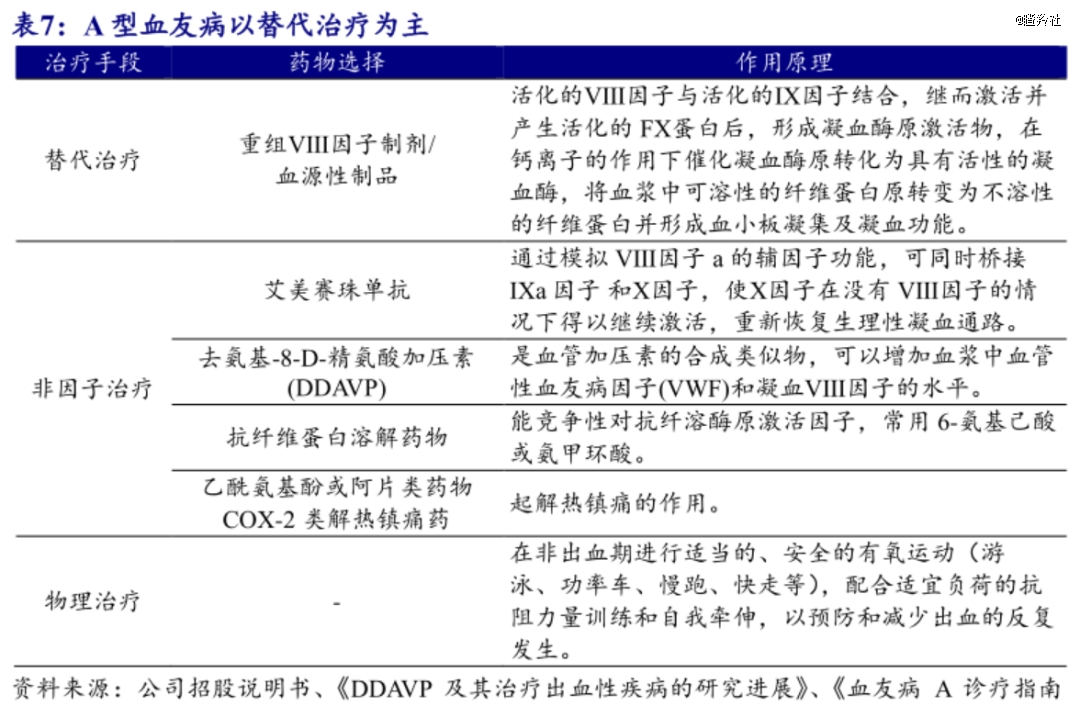
由于血友病是基因导致的遗传性疾病,所以患者需要终身注射凝血因子(治标不治本),血友病患者至少需要每周注射一到两次凝血因子,以维持正常的凝血功能这也催生了庞大的血友病用药市场。
据贝哲斯咨询数据预测:2028年全球血友病治疗药物市场规模将达1102.25亿元,2023-2028年CARG为8.62%。
据第三方机构数据显示,中国血友病用药市场预计2023年将达到55.2亿元人民币,2030年将达到141亿元人民币,期间年化增长率为22.5%。
这一庞大而快速增长的药物市场,固然催生出了如罗氏的重组人源化IgG4双抗艾美赛珠单抗这样的重磅药物,但目前短效重组VIII因子仍然是可及性高、性价比高的选择,仍需更具可及性和疗效优异的产品来洗牌市场。
在美国,长效八因子年治疗费用约15万美元(按中剂量测算)、艾美赛珠单抗年治疗费用超过50万美元,基因疗法Roctavian更是定价290万美元一针;视角回到国内,艾美赛珠单抗未经医保价格同样高昂,反倒是长效重组八因子更具备性价比优势。
2、罗氏双抗迎来强大挑战
罗氏的Hemlibra能取得如此大的优势和战果,除了它占据了A型血友病创新药物的先发优势外,还有解决了诸多未满足需求:
1)注射凝血因子VIII预防至少每周注射3-4次(长效凝血因子1-2次),均需要静脉注射;Hemlibra只需要每周注射一次,并且是皮下注射,大大提升了患者的依从性;
2)对于伴有凝血因子Ⅷ抑制物的A型血友病患者来说(50-60%的血友病A患者在注射凝血因子VIII制品之后会产生凝血因子VIII的抑制物),通过凝血因子Ⅷ进行常规预防和止血治疗不再有效,旁路途径药物(BPA)和长时间大剂量使用凝血因子Ⅷ进行诱导免疫耐受(ITT)进行治疗,Hemlibra提供了一个全新的选择;
3)使用Hemlibra治疗可显著降低患者的年化出血事件(ABR)。HAVEN系列临床数据汇总显示:存在或不存在因子VIII抑制剂的所有年龄段A型血友病患者中,高比例患者接受Hemlibra治疗经历零治疗出血,维持中位时间83周;超过87%患者无关节出血(自发性或因受伤/创伤)、超过92%患者从第25周开始每个时间间隔内没有自发性出血。
Hemlibra在疗效层面已经做到较高水准,目前多数的替代竞品均从药物的半衰期入手,以图提升患者的依从性。
诺和诺德mim8是新一代的FIXa/FX双抗,被市场认为是Hemlibra上市以来最强的竞争对手之一。
从多个维度来看,mim8可能对比Hemlibra具有潜在优势的有两大方面:
1)mim8在每月注射一次的患者ABR或零出血率指标上可能优于Hemlibra;
2)在部分A型血友病患者群体中,mim8临床数据也展现出了潜在优于Hemlibra的潜力。比如先前接受过凝血因子VIII预防治疗的患者中,Mim8每周给药组中零治疗性出血的患者比例为66%,Hemlibra每周给药组的54%(HAVEN-3研究),每月给药时,Mim8和Hemlibra的这一比例分别为65%和56%;
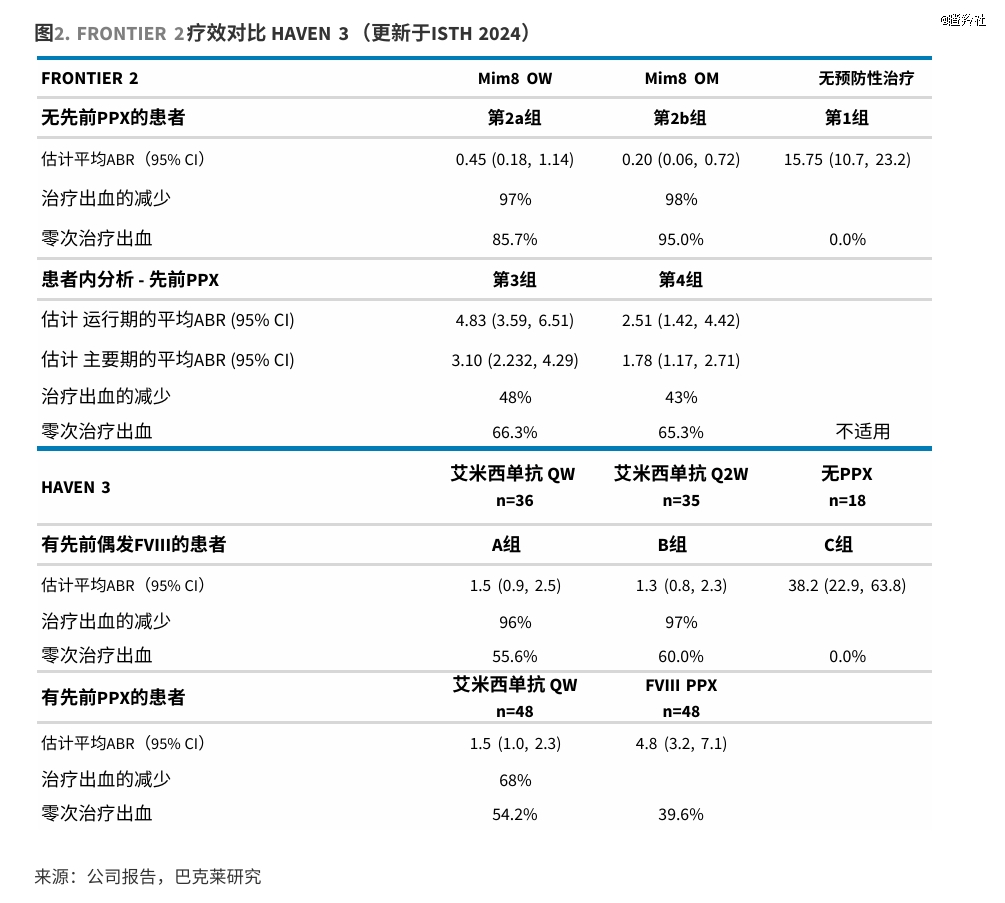
辉瑞的产品组合同样具备一定竞争力。
TFPI抗体马塔西单抗(每周一次、皮下注射)的机制与FIXa/FX双抗完全不同,抑制TFPI来活化FVIIa和FX实现止血功能的恢复。在面对无法继续接受因子替代疗法的A型或者B型血友病患者中,仍能通过TFPI抗体注射来实现止血功能的恢复。
BASIS研究显示,在重度A型血友病和中度至重度B型血友病患者中,与按需静脉注射方案相比,该药物可将年化出血率降低92%;与凝血因子预防给药治疗相比,该药物可将年化出血率降低35%。
与Sangamo合作的A型血友病基因疗法更是备受关注,最新公布的三期AFFINE研究数据显示:患者在一次性静脉注射后,从第12周到至少第15个月,在年化出血率(ABR)方面相较于常规FVIII预防治疗显示非劣效性和优效性。从第12周到至少第15个月,平均总ABR较注射前降低了74%,从基线到中位数3年随访期间,平均总ABR降低了52%。
不过这种基因疗法并非一劳永逸,后续仍需新一轮补充注射。同时安全性也令人有所担忧,15名患者(20%)报告了严重不良事件(SAE),其中10名患者(13.3%)的13起事件被认为与治疗相关。
从海外主流市场观点来看,分析师和投资者普遍还是对诺和诺德的mim8寄予厚望,认为其峰值能够给公司带来近30亿美元的年收入。
3、国内的机会
国内药物厂商的主战场仍然在替代治疗产品重组凝血因子VIII这个维度上,Biotech神州细胞因重组VIII因子SCT8000的大卖而实现扭亏为盈,这也鼓舞了许多研发血友病药物的药企,陆续有更多药企加入商业化战局(正大天晴、成都蓉生)。
国内对于FIXa/FX双抗的布局严重缺位,但罗氏的Hemlibra已在国内上市,诺和诺德mim8正在快速推进临床。
反倒是TFPI抗体和血友病基因疗法层面,国内有Biotech进行跟进布局。
7月24日,信念医药向NMPA提交BBM-H901注射液治疗B型血友病成年患者的NDA,是国内*递交新药上市申请的针对遗传病的基因治疗药物。
BBM-H901采用静脉给药将人凝血因子IX基因导入B型血友病患者体内持续表达,提高并长期维持患者的凝血因子水平。其公布IIT研究的临床数据也十分惊艳,10例受试者在输注BBM-H901后,随访时间为3.0-4.5年,各时间点平均FIX活性>30%;10例中的9例受试者FIX持续稳定较高表达,未发生出血事件,年化出血率(ABR)为0,且完全停止了外源性FIX产品的替代治疗。同时,安全性良好,无严重不良事件、无血栓栓塞事件等安全性信号。
早在去年10月,信念医药就将中国商业化权益授予武田。
TFPI抗体领域,目前苏州康宁杰瑞的KN057和安源医药的AP017分别处于二期和一期临床阶段,是国内研发进度前二的TFPI抗体。
值得注意的是,苏州康宁杰瑞并不在上市公司体内,而KN057大中华区权益早在去年9月被苏州康宁杰瑞授出给远大生命科学,远大生命科学将支付累计最高人民币5亿元的权益付款(包括首付款和里程碑款)。
从最新发布的KN057临床数据看,KN057大概率是辉瑞马塔西单抗的follow或者me better(半衰期在一周左右、皮下注射),数据展现了该分子对无论有无抑制物的A型血友病或B型血友病患者血浆中的作用趋势和有效作用浓度范围基本一致。
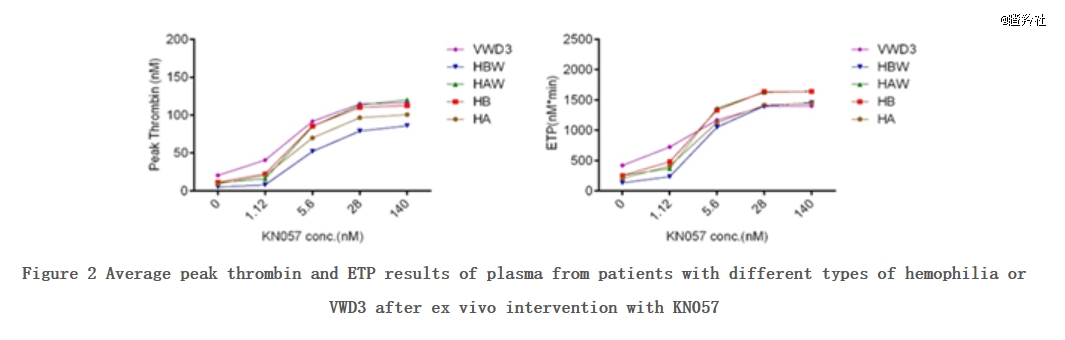
结语:越来越多血友病新型药物的攻擂,可能显著影响药物格局的变化和影响大药企的兴衰(Hemlibra过去常年占据罗氏第二大收入药物位置)。面对这样“不罕见的罕见病”,也期待国内出现更多像信念医药一样敢于做FIC或者BIC的Biotech。
【本文由投资界合作伙伴瞪羚社授权发布,本平台仅提供信息存储服务。】如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。





